Les anticoagulants jouent un rôle majeur dans la prise en charge des maladies vasculaires du foie (MVF). Leur utilisation est cependant délicate en raison de l’hypertension portale fréquemment retrouvée dans ces pathologies. L’hypertension portale entraîne un risque accru d’hémorragie par rupture de varices œsophagiennes (VO) mais également par la présence fréquente d’une thrombopénie. Par ailleurs, lorsque la pathologie est associée à une insuffisance hépatique, les anomalies de l’hémostase observées compliquent encore l’utilisation des anticoagulants. Enfin, en cas de résection digestive secondaire à une ischémie mésentérique, l’absorption des traitements anticoagulants oraux et leur pharmacocinétique posent de nombreuses questions. Le rapport bénéfice/risque hémorragie/thrombose du traitement doit donc être soigneusement évalué. Cependant, les études sont peu nombreuses et souvent de faible niveau de preuve dans ces pathologies rares. Le traitement est adapté le plus souvent au cas par cas selon la pathologie : syndrome de Budd-Chiari (SBC), thrombose veineuse portale (TVP), maladie vasculaire porto-sinusoïdale (MVPS), facteurs de risque de thrombose retrouvés et évolution des connaissances.
Principes généraux du traitement anticoagulant dans les maladies vasculaires du foie
Le traitement anticoagulant des MVF est crucial pour prévenir l’extension de la thrombose, favoriser la reperméabilisation et réduire le risque de complications graves telles que l’hypertension portale et l’ischémie mésentérique. Il doit être mis en place le plus rapidement possible. Compte tenu de l’hypertension portale, le traitement des varices œsophagiennes doit être systématique lors de l’instauration du traitement, bien que les études aient montré que les anticoagulants n’augmentent pas le risque d’hémorragie digestive due à l’hypertension portale chez ces patients.1,2
La thrombopénie est le plus souvent modérée et ne doit pas faire modifier ou arrêter le traitement anticoagulant. Une thrombopénie sévère (inférieure à 50 G/L) nécessite une surveillance étroite et une prise en charge dans un centre spécialisé.3
Au cours du SBC, l’insuffisance hépatique peut entraîner une diminution de la synthèse des facteurs de la coagulation (facteurs procoagulants [FII, FV…] mais également inhibiteurs de la coagulation comme l’antithrombine [AT], la protéine C [PC] et la protéine S [PS]), permettant un certain rééquilibrage de la balance hémostatique. L’allongement des temps de coagulation (temps de céphaline activée [TCA]) et la diminution du taux de prothrombine (TP) ne permettent pas d’évaluer ces modifications et ne doivent surtout pas contre-indiquer ou différer le traitement anticoagulant. En cas d’atteinte de la fonction hépatique avec coagulopathie, l’indication du traitement doit être soigneusement pesée et le suivi doit être rigoureux, pluridisciplinaire au sein d’une équipe spécialisée.
Les femmes en âge de procréer doivent être informées des risques du traitement anticoagulant en cas de grossesse et au cours de l’allaitement. En cas de désir de grossesse, celle-ci doit être planifiée et suivie par une équipe multidisciplinaire : obstétricien, hépatologue, hématologue.4 Les ménorragies sont fréquentes et parfois invalidantes, nécessitant une prise en charge adaptée.
Tous les patients doivent bénéficier d’une éducation thérapeutique leur permettant de connaître les caractéristiques, les risques du traitement, les précautions à prendre dans la vie courante et dans les situations à risque ainsi que les signes d’alerte et les conduites à tenir.
Cette prise en charge nécessite une étroite collaboration entre les hépatologues, les gastroentérologues, les radiologues et les spécialistes de l’hémostase.
Médicaments anticoagulants utilisés
Héparine non fractionnée et héparine de bas poids moléculaire
Les héparines constituent le traitement le plus fréquemment utilisé à la phase aiguë de la TVP ou du SBC. Ces médicaments agissent indirectement en se liant à l’antithrombine pour amplifier l’inhibition de la thrombine et/ou du facteur Xa. Leur surveillance peut être effectuée en mesurant l’activité anti-Xa et elles sont administrées par voie sous-cutanée ou intraveineuse.
La complication redoutée du traitement héparinique est la thrombopénie induite par l’héparine (TIH) qui associe une diminution des plaquettes et la survenue de thromboses (lire l’article « De la thrombopénie induite par l’héparine à l’émergence de syndromes de thrombopénie thrombotique immune » dans La Revue du Praticien d’octobre 2025). Elle est plus fréquente avec les héparines non fractionnées (HNF) qu’avec les héparines de bas poids moléculaire (HBPM) et nécessite une surveillance de la numération plaquettaire lors de l’instauration du traitement. La TIH apparaît entre le cinquième et le vingt et unièmejour de traitement et nécessite un arrêt immédiat de l’héparine et un traitement curatif par un anticoagulant substitutif comme le danaparoïde sodique ou l’argatroban. L’incidence de la TIH est plus élevée chez les patients atteints de maladie vasculaire du foie, en particulier au cours du syndrome myéloprolifératif , cause fréquente des MVF. L’utilisation des HNF est donc à éviter chez ces patients.5
En cas d’insuffisance hépatique, l’efficacité de l’héparine peut être affectée par les faibles niveaux d’antithrombine ;6 la surveillance de l’activité anti-Xa permet de mettre en évidence une diminution importante de l’antithrombine (AT) et doit être surveillée chez ces patients afin optimiser le traitement.
Antivitamines K
Les antivitamines K (AVK) inhibent la synthèse de facteurs de coagulation dépendant de la vitamine K (II, VII, IX et X). En raison de leur délai d’action, ils nécessitent un relais avec l’héparine et une adaptation de dose par mesure de l’international normalized ratio (INR). De plus, l’indice thérapeutique étroit et les interactions alimentaires et médicamenteuses significatives de ces traitements nécessitent une surveillance biologique pour maintenir un temps dans l’intervalle thérapeutique (time in therapeutic range [TTR]) optimal.
Ils ont des antidotes disponibles : la vitamine K et le concentré de complexe prothrombinique en cas d’urgence.
La surveillance de l’INR peut se faire au laboratoire mais également par automesure à domicile, permettant ainsi une amélioration de la qualité de vie des patients.
Comme pour les héparines, en cas d’insuffisance hépatique, le traitement par AVK est particulièrement difficile à utiliser en raison d’un INR de base parfois élevé. Lorsque la coagulopathie est sévère (facteur V inférieur à 50 %, fibrinogène inférieur à 1 g/L) ou que l’INR avant traitement est supérieur à 1,5, une prise en charge par une clinique des anticoagulants et/ou des services spécialisés est nécessaire.
Pour les femmes en âge de procréer, il important de rappeler que les AVK sont contre-indiqués dès la huitième semaine d’aménorrhée. Il faut donc informer les patientes et leur indiquer la conduite à tenir en cas de grossesse.
Anticoagulants oraux directs
Les anticoagulants oraux directs (AOD) ciblent directement et spécifiquement soit la thrombine (dabigatran), soit le facteur Xa (rivaroxaban, apixaban). Ils ont de nombreux avantages comparés aux AVK : ils sont efficaces immédiatement, ont une demi-vie courte, leur fenêtre thérapeutique est large, il n’y a pas d’interactions alimentaires et peu d’interactions médicamenteuses, et ils sont principalement éliminés par le rein et le foie (tableau 1). Les AOD ont montré dans les études pivots une efficacité comparable à celle des AVK et sont donc aujourd’hui recommandés en première intention pour le traitement de la thrombose veineuse profonde et de l’embolie pulmonaire.7
Les AOD sont administrés une ou deux fois par jour par voie orale, à dose fixe, et ne nécessitent pas de suivi biologique. Il est cependant recommandé de surveiller l’hémogramme, la fonction rénale et hépatique chez les patients traités au long cours, avec une périodicité à adapter selon les comorbidités du patient.
Les tests de coagulation ne permettent pas d’évaluer un traitement par AOD. En effet, leurs interférences avec le TP et/ou le TCA sont inconstantes et variables. Ainsi, un bilan normal n’exclut pas un traitement par AOD, et une perturbation de ces tests ne permet pas d’évaluer l’efficacité du traitement. Il existe des dosages spécifiques des AOD qui ne sont pas recommandés en dehors de situations telles qu’une intervention chirurgicale urgente ou la survenue d’une hémorragie. Compte tenu de leur pharmacocinétique, les AOD ne nécessitent pas de relais. Seul le dabigatran dispose d’un antidote en France actuellement. Cependant, les études montrent que la morbidité et la mortalité au cours des hémorragies ne sont pas différentes chez les patients traités par AOD versus par AVK.8
Les patients avec une atteinte hépatique ont été systématiquement exclus des études pivots et aucune n’a inclus de patients avec une MVF. Les AOD ont cependant montré leur efficacité et leur sécurité au cours de la cirrhose et sont autorisés avec précaution dans les cirrhoses CHILD A et B (sauf le rivaroxaban).1 Quelques études récentes ont montré que les AOD semblent efficaces et sûrs dans les MVF et en particulier au cours de la thrombose veineuse porte, en relais de l’héparine ou en remplacement des AVK ;9 des études prospectives sont néanmoins nécessaires. Il n’y a pas de travaux sur la modification de la pharmacocinétique en cas de shunt portosystémique intrahépatique (TIPS).
L’absorption des AOD se fait en partie au niveau de l’intestin grêle ; il n’y a pas actuellement de données sur leur absorption en cas de grêle court lié à une résection digestive secondaire à l’ischémie mésentérique. Leur utilisation ne peut donc pas être recommandée actuellement chez ces patients.10
Les AOD ne sont pas recommandés au cours du syndrome des antiphospholipides (SAPL), tout particulièrement triple positif, car ils ont montré une efficacité moindre que celle des AVK et sont contre-indiqués dans l’insuffisance rénale sévère.11
Enfin, pour les femmes en âge de procréer, les AOD sont contre-indiqués pendant toute la grossesse et au cours de l’allaitement. Il faut donc informer les patientes et leur indiquer la conduite à tenir en cas de grossesse.
Modalités de traitement selon la pathologie
Syndrome de Budd-Chiari
Le traitement anticoagulant au cours du SBC doit être initié dès que possible.1,12 Une HBPM à dose thérapeutique, suivie par un AVK, avec un INR cible entre 2 et 3 est actuellement le traitement de première intention. Comme évoqué précédemment, lorsque la coagulopathie est sévère avec un INR de base élevé avant traitement, il est difficile d’évaluer de manière fiable l’effet anticoagulant.
L’HNF est à éviter compte tenu du risque accru de thrombopénie induite par l’héparine au cours du SBC.
L’utilisation des AOD au cours du SBC n’est pas recommandée aujourd’hui par manque de données. Leur utilisation va probablement augmenter dans les années à venir, car ils semblent efficaces et sûrs dans cette indication d’après de rares études rétrospectives sur de faibles effectifs.1,13 Leur utilisation dans cette indication nécessite un avis en réunion de concertation pluridisciplinaire (RCP) et un suivi multidisciplinaire spécialisé.
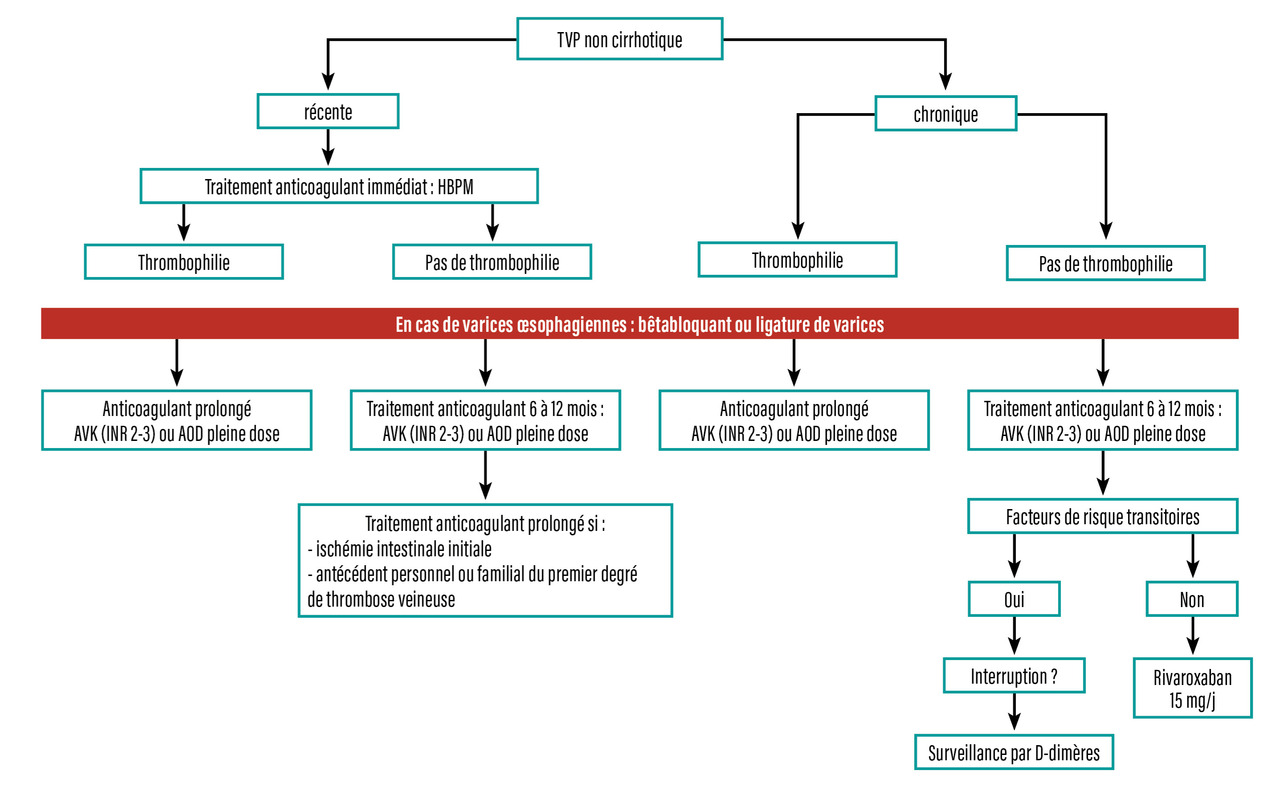
Thrombose veineuse porte non cirrhotique
À la phase aiguë de TVP, le traitement anticoagulant doit être initié dès que possible.1,12 Les HBPM à dose curative sont le traitement actuellement recommandé. Les HNF ne doivent pas être utilisées du fait d’un risque accru de TIH. Elles peuvent être utilisées en milieu hospitalier en cas d’ischémie aiguë mésentérique sévère.
Les AVK peuvent être utilisés pour le traitement à long terme en relais des HBPM, avec une cible de l’INR entre 2 et 3.
Les AOD peuvent être utilisés en relais des héparines. Les quelques études disponibles indiquent une efficacité comparable à celle des AVK, tout en étant associée à un risque hémorragique réduit.9 En cas de résection digestive, en raison du manque de données sur l’absorption des AOD, les AVK sont alors utilisés en première intention. Cependant, compte tenu des difficultés fréquentes liées aux troubles digestifs et d’adaptation de l’INR, un suivi dans une équipe spécialisée est alors souhaitable.
La durée du traitement anticoagulant au cours de la TVP reste un sujet discuté. En cas de thromboses idiopathiques, de thrombophilie sévère, de SMP, de TVP étendue avec présence d’une ischémie mésentérique, un traitement par AVK ou AOD prolongé est indiqué.
En cas de TVP provoquée par un facteur déclenchant, une anticoagulation d’au moins six mois est indiquée. Selon une étude récente (RIPORT), il a été montré qu’une anticoagulation par rivaroxaban 15 mg chez les patients avec TVP ancienne et sans facteur de risque prothrombotique réduit le risque de récidive de thrombose de manière significative.14
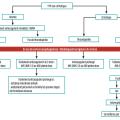
La durée, la molécule, les posologies, les modalités de surveillance peuvent être discutées en RCP afin d’adapter au cas par cas le traitement (fig. 1).
Maladies vasculaires porto-sinusoïdales
La TVP est une complication fréquente des MVPS, tant au moment du diagnostic que lors du suivi. Dans la plus grande et la plus récente série de MVPS, environ 29,5 % des patients ont présenté une TVP.15 Compte tenu de ce risque fréquent, l’utilisation de l’anticoagulation prophylactique pour prévenir le développement de la TVP a fait l’objet de discussions ces dernières années. Les résultats de l’étude APIS sont attendus pour soumettre des recommandations.
À ce jour, l’anticoagulation prophylactique, dans le but de prévenir le développement de la TVP dans les MVPS, n’est pas recommandée. En revanche, une surveillance radiologique sur la perméabilité de la veine porte est recommandée tous les six mois par échographie Doppler hépatique.1
Gestion périopératoire des anticoagulants
Les patients ayant une MVF sont régulièrement soumis à des gestes invasifs, comme l’endoscopie, la revascularisation endovasculaire, la pose de TIPS… Ces gestes à risque hémorragique nécessitent un encadrement rigoureux.
La gestion des anticoagulants doit prendre en compte plusieurs facteurs :
- le risque lié au patient (thrombopénie, présence de comorbidités, insuffisance rénale, insuffisance hépatique, prise d’antiagrégants, l’ancienneté de la thrombose…) ;
- le risque lié au geste ;
- l’expérience de l’opérateur ;
- le plateau technique disponible (transfusion, laboratoire, radiologie interventionnelle…).
Les recommandations sur la gestion périopératoire des anticoagulants de la population générale s’appliquent chez les patients avec une MVF. Il faut cependant être particulièrement vigilant aux risques hémorragiques liés à la thrombopénie et à l’éventuelle insuffisance hépatique. De même, le risque thrombotique de la pathologie est très différent entre une TVP ancienne non compliquée et une pathologie thrombotique sévère récente et/ou récidivante.
Par exemple, une ponction d’ascite, geste à faible risque hémorragique, peut nécessiter un arrêt de traitement chez un patient avec un SBC sévère. Tout geste nécessite donc une évaluation rigoureuse du risque hémorragie/thrombose.
Il est essentiel que les patients sous anticoagulants soient sensibilisés aux risques des gestes invasifs. Les arrêts, relais et surveillances doivent être bien expliqués aux patients, un protocole écrit clair est recommandé (fig. 2). Ceci est particulièrement important pour les gestes tels qu’extractions dentaires, infiltrations… car souvent réalisés en ville, mais également pour les gestes plus invasifs car les précautions sont généralement à prendre en amont de l’hospitalisation. La bonne compréhension par le patient est un gage de sécurité. La carte mentionnant la prise d’un traitement anticoagulant est particulièrement utile dans ces situations pour informer les différents professionnels de santé qui prennent en charge le patient.
Gestion des AVK en périopératoire
Selon les recommandations de la Société française d’anesthésie et de réanimation 2008,16 les actes tels que chirurgie cutanée, endoscopies et actes buccodentaires, ponction d’ascite, infiltration/ponction d’une articulation périphérique…, considérés à faible risque hémorragique, peuvent être réalisés sans interruption des AVK. Il faut cependant vérifier avant le geste que l’INR est bien dans la zone thérapeutique et l’opérateur doit être averti du traitement, afin d’adapter éventuellement son geste (hémostase locale).
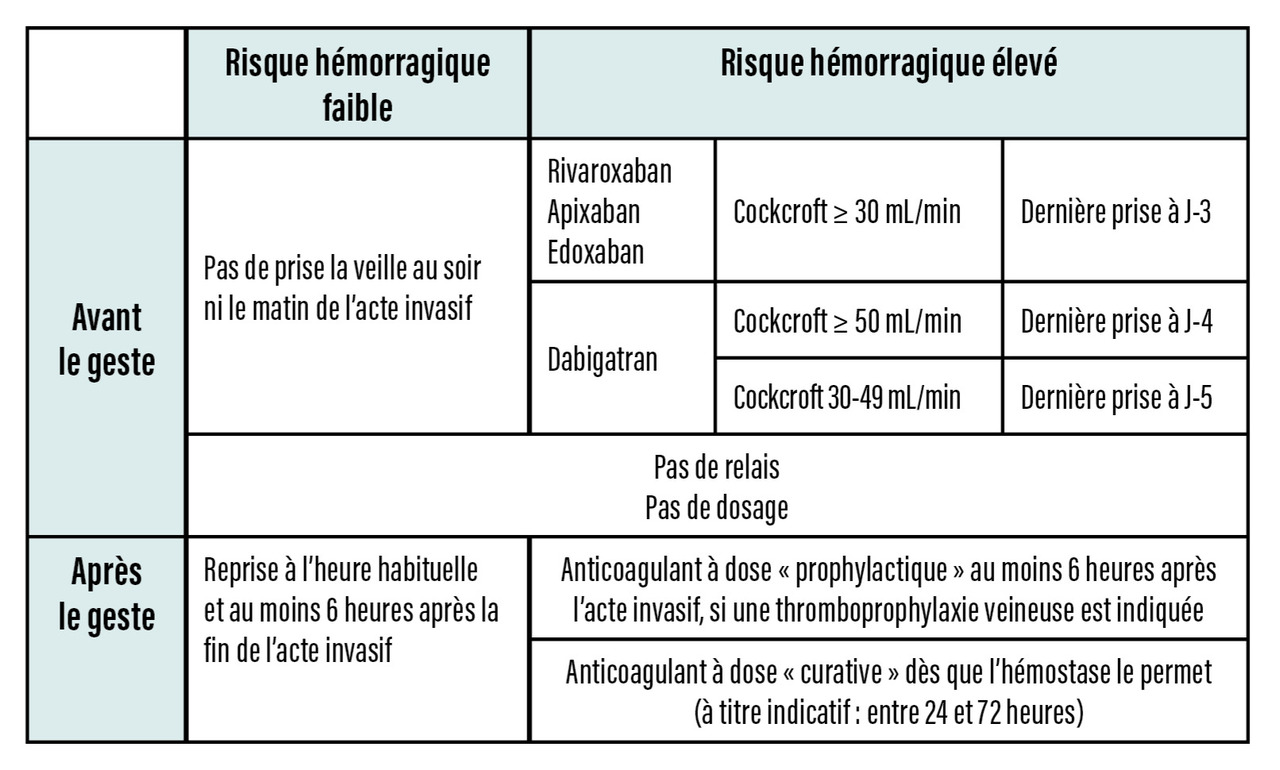
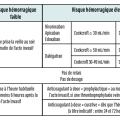
Si le risque hémorragique lié au patient (thrombopénie sévère, atteinte hépatique) ou lié à la procédure elle-même est particulièrement élevé, alors le traitement par AVK peut être interrompu, le plus souvent sans relais préopératoire, sauf en cas de risque thrombotique élevé (thrombose récente étendue, ischémie mésentérique, SAPL…) [tableau 2].
Deux modalités sont à respecter pour l’arrêt des AVK :
- arrêt cinq jours avant l’intervention sans relais héparinique en préopératoire, sauf en cas de risque thrombotique élevé, relais par HBPM avec mesure de l’INR la veille de l’opération ;
- reprise des AVK systématiquement en relais de l’héparine.
Gestion des AOD
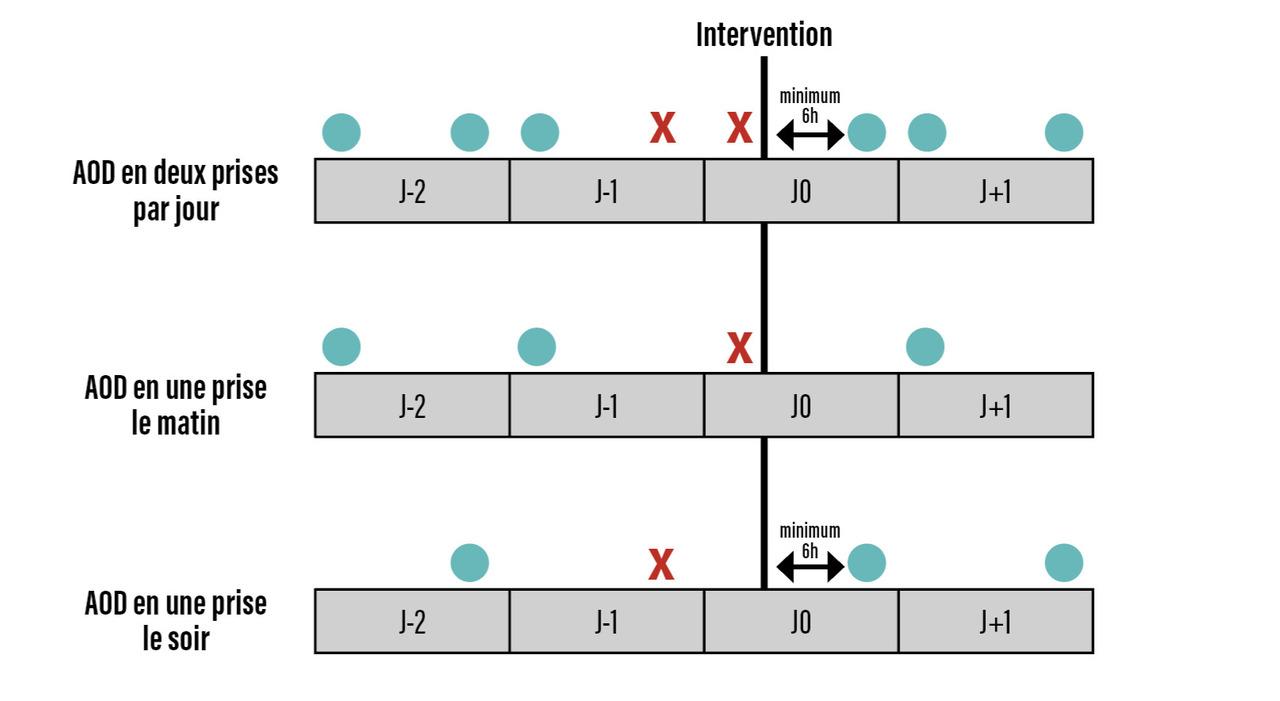
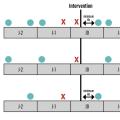
Selon le Groupe d’intérêt en hémostase périopératoire 2016,17 la gestion périopératoire des AOD, compte tenu de leur demi-vie et de leur rapidité d’action, est beaucoup plus simple et ne nécessite pas de relais. En pratique, selon le risque de la chirurgie et de la fonction rénale, plusieurs schémas d’arrêt sont proposés (fig. 3 et 4).
La reprise des AOD se fait généralement entre vingt-quatre et soixante-douze heures après le geste selon l’hémostase locale, le risque de reprise chirurgicale et l’opérateur. Avant la reprise, on peut administrer une dose prophylactique d’HBPM selon le risque thrombotique du patient.
Clinique des anticoagulants et éducation thérapeutique
Même si les cliniques des anticoagulants (CAC) n’ont pas été créées spécifiquement pour les MVF, elles sont utiles pour l’accompagnement de ces patients. à l’origine, ces structures ont été mises en place pour la surveillance des AVK, avec pour objectifs une (télé)surveillance des INR et une éducation thérapeutique des patients aux anticoagulants. Elles ont montré leur efficacité et sont largement développées dans les pays nordiques mais sont malheureusement encore rares en France.18 Aujourd’hui, les CAC, outre le suivi des AVK, ont inclus le suivi des AOD, en particulier dans leur programme d’éducation thérapeutique du patient (ETP). La surveillance des AVK est aujourd’hui largement améliorée par la détermination de l’INR à l’aide d’appareils d’automesure remboursés depuis 2023, permettant une autonomisation plus grande des patients et l’amélioration de leur qualité de vie. Leur utilisation nécessite un apprentissage, qui peut être effectué dans la CAC.
Exemple de suivi des INR de la CAC de l’hôpital Beaujon
Les patients sont adressés par les médecins du centre de référence des MVF. Après une consultation pour inclusion, les INR déterminés par automesure ou par le laboratoire de ville sont transmis à la CAC ; l’adaptation du traitement, la date du prochain contrôle sont alors fixés à l’aide d’un logiciel développé par le Dr Cambus (CHU de Toulouse). La conduite à tenir est transmise le jour même au patient. En cas de geste médical, les protocoles d’arrêt et/ou de relais peuvent être également effectués à distance. La CAC est accessible aux patients pour répondre à leurs questions ainsi qu’aux médecins qui suivent les patients.
Éducation thérapeutique en collaboration avec les associations de patients
L’ETP sous anticoagulants est essentielle ; elle doit leur permettre d’acquérir des compétences souvent complexes, ce qui nécessite un parcours spécifique. Selon la Haute Autorité de santé, l’ETP a pour but « d’aider les patients à acquérir ou maintenir les compétences dont ils ont besoin pour gérer au mieux leur vie avec une maladie chronique ». Le programme d’ETP de la CAC de Beaujon a été développé en collaboration avec l’Association des malades des vaisseaux du foie, partenaire essentiel du programme. L’équipe d’ETP est pluridisciplinaire, regroupant infirmiers, pharmaciens, médecins, patients experts. Des séances individuelles et des ateliers sont proposés permettant de répondre aux besoins de chaque patient. Le programme est ainsi adapté pour chacun après un entretien individuel qui a pour but de déterminer ses besoins et ses attentes (qualité de vie, vie familiale, sociale, professionnelle…) et qui peuvent différer des priorités envisagées par les médecins (observance) : c’est le diagnostic éducatif. Des outils ont été développés au sein de la CAC Beaujon tels que des livrets d’éducation thérapeutique, un jeu de l’oie et des jeux éducatifs accessibles sur smartphone ou ordinateur pour une autoévaluation des connaissances (fig. 5) [lire l’article « Vivre avec une maladie des vaisseaux du foie » dans La Revue du Praticien de janvier 2024].
Le programme d’ETP a pour objectif la compréhension de la maladie, la connaissance des caractéristiques du traitement anticoagulant, de ses risques, des modes de surveillance, des signes d’alerte et des réactions à avoir dans les situations d’urgence. L’ETP doit permettre une meilleure adhésion au traitement et une amélioration de la qualité de vie des patients.
2. Guillaume M, Christol C, Plessier A, et al. Bleeding risk of variceal band ligation in extrahepatic portal vein obstruction is not increased by oral anticoagulation. Eur J Gastroenterol Hepatol 2018;30(5):563-8.
3. Delgado MG, Seijo S, Yepes I, et al. Efficacy and safety of anticoagulation on patients with cirrhosis and portal vein thrombosis. Clin Gastroenterol Hepatol 2012;10(7):776-83.
4. Payancé A, Ceccaldi PF, De Raucourt E, et al. Pregnancy and vascular liver diseases: Vascular liver diseases: Position papers from the francophone network for vascular liver diseases, the French Association for the Study of the Liver (AFEF), and ERN-rare liver. Clin Res Hepatol Gastroenterol 2020;44(4):433-7.
5. Randi ML, Tezza F, Scapin M, et al. Heparin-induced thrombocytopenia in patients with Philadelphia-negative myeloproliferative disorders and unusual splanchnic or cerebral vein thrombosis. Acta Haematol 2010;123(3):140-5.
6. Bechmann LP, Wichert M, Kröger K, et al. Dosing and monitoring of low-molecular-weight heparin in cirrhotic patients. Liver Int 2011;31(7):1064.
7. Tripodi A, Palareti G. New anticoagulant drugs for treatment of venous thromboembolism and stroke prevention in atrial fibrillation. J Intern Med 2012;271(6):554-65.
8. Ruff CT, Giugliano RP, Braunwald E, et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: A meta-analysis of randomised trials. Lancet 2014;383(9921):955-62.
9. Naymagon L, Tremblay D, Zubizarreta N, et al. The efficacy and safety of direct oral anticoagulants in noncirrhotic portal vein thrombosis. Blood Adv 2020;4(4):655-66.
10. Martin KA, Lee CR, Farrell TM, et al. Oral anticoagulant use after bariatric surgery: A literature review and clinical guidance Am J Med 2017;130(5):517-24.
11. Benhamou Y, Delluc A, Fischer AM, et al. Quelles sont les particularités thérapeutiques au cours du syndrome des antiphospholipides ? Rev Mal Respir 2019.
12. Elkrief L, Payance A, Plessier A, et al. Management of splanchnic vein thrombosis. JHEP Rep 2023;5(4):100667.
13. Semmler G, Lindorfer A, Schäfer B, et al. Outcome of Budd-Chiari syndrome patients treated with direct oral anticoagulants: An Austrian multicenter study. Clin Gastroenterol Hepatol 2023;21(4):978-987.e2.
14. Plessier A, Goria O, Cervoni JP, et al. Rivaroxaban prophylaxis in noncirrhotic portal vein thrombosis. NEJM Evid 2022;1(12):EVIDoa2200104.
15. Magaz M, Giudicelli-Lett H, Abraldes JG, et al. Porto-sinusoidal vascular liver disorder with portal hypertension: Natural history and long-term outcome. J Hepatol 2025;82(1):72-83.
16. Godier A, Pernod G, Sie P. Gestion péri-opératoire des AVK : recommandations 2008. Mapar 2009;331-9.
17. Albaladejo P, Bonhomme F, Blais N, et al. Gestion des anticoagulants oraux directs pour la chirurgie et les actes invasifs programmés : propositions réactualisées du Groupe d’intérêt en hémostase périopératoire (GIHP) – septembre 2015. Anesth Reanimation 2016;2(6):414-20.
18. Cambus JP, Magnin D, Ambid-Lacombe C, et al. Anticoagulant clinics are they effective in France? Performance evaluation of six anticoagulant clinics concerning the management of vitamin K antagonists. Rev Med Interne 2013;34(9):515-21.